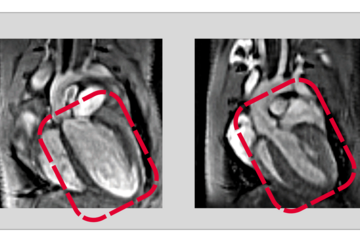
Mechanismus zur Behandlung von Muskelschwund entdeckt
Utrophin-Anstieg in Muskelzellen nach transkriptionaler Adaptation normalisiert Zellfunktion bei Duchenne Muskeldystrophie
Die Duchenne Muskeldystrophie ist eine seltene Erbkrankheit mit schwerwiegenden Folgen wie Muskelschwund. Verursacht wird dies durch bestimmte Mutationen im Dystrophin-Gen, infolge dessen die Genexpression gestört ist. Dadurch werden lediglich mRNA-Fragmente statt intakter mRNA-Ketten gebildet. Forscher vom Max-Planck-Institut für Herz- und Lungenforschung zeigten nun, dass mittels einer Regulation des weiteren Abbaus der mRNA-Fragmente, einer transkriptionellen Adaptation, vermehrt Utrophin gebildet wird, womit das fehlende Dystrophin kompensiert werden kann. Die Wissenschaftler halten die Studie für bahnbrechend, da sie den Weg für neue Therapieansätze bei der Duchenne Muskeldystrophie, aber auch andere genetisch bedingte Erkrankungen ebnen könnte.
Bei der Duchenne Muskeldystrophie (DMD) handelt es sich um eine schwere Muskelerkrankungen, die vor allem Jungen betrifft. Die Erkrankung verläuft chronisch und beginnt bereits im Kindesalter. Die Lebenserwartung bei den betroffenen Patienten ist deutlich verkürzt. Verursacht wird die bislang nicht heilbare Erkrankung durch Mutationen im Dystrophin-Gen. Dieses liegt auf dem X-Chromosom. Dystrophin ist für die Stabilität der Zellmembran in Muskelfasern wichtig. Durch den Gendefekt fehlt den Patienten Dystrophin, so dass die Muskelzellen in ihrer Funktion eingeschränkt sind und die Muskulatur zunehmend geschwächt wird.
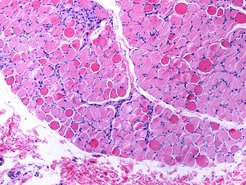
Die Behandlung von Duchenne Muskeldystrophie beschränkt sich bislang in der Regel darauf, mit geeigneten Verfahren die Muskelfunktion so lange wie möglich zu erhalten. Zudem werden erste Gentherapien eingesetzt, mit denen die Produktion von Dystrophin in den Muskelzellen gesteigert werden soll.
Wissenschaftlerinnen und Wissenschaftler aus der Abteilung „Genetik der Entwicklung“ von Didier Stainier am Max-Planck-Institut für Herz- und Lungenforschung in Bad Nauheim haben nun in einer Studie entscheidende neue Erkenntnisse über die genetischen Zusammenhänge bei der Entstehung der DMD gefunden, welche die Grundlage für neue therapeutische Ansätze darstellen könnten.
Im Zentrum steht dabei neben Dystrophin ein zweites Protein namens Utrophin. Beide Proteine sind miteinander verwandt.
„Bereits früher war bekannt, dass eine vermehrte Produktion von Utrophin fehlendes Dystrophin zumindest in Teilen kompensieren kann“, so Lara Falcucci, Erstautorin der Studie. „Wir konnten nun erstmals in menschlichen Muskelzellen zeigen, dass auf der Ebene der Genexpression ein als transkriptionale Adaptation bezeichneter Prozess dazu in der Lage ist, die Produktion von Utrophin zu verstärken.“
Bislang war dies nur von tierischen Organismen, wie dem Fadenwurm C. elegans, Zebrafisch oder Maus bekannt.
„Um den Mechanismus zu verstehen, ist es wichtig zu wissen, dass bei DMD das Dystrophin-Gen zwar vorhanden ist. Verschiedene Mutationen verhindern jedoch die Produktion eines funktionalen Genprodukts, also eines Proteins. Zusätzlich verursachen einige die Dystrophin-Mutationen, dass die vom Gen transkribierte mRNA in Fragmente zerfällt. Diese wiederum übernehmen überraschenderweise neue Funktionen bei der Regulation anderer Gene," erklärt Mitautor Christopher Dooley.
Die Max-Planck-Wissenschaftler zeigten nun an kultivierten Zellen von DMD-Patienten, dass die Dystrophin-mRNA-Fragmente in den Zellen eine verstärkte Produktion von Utrophin verursachen. „Der Mechanismus dahinter ist die transkriptionale Adaptation. Wenn man den Zerfallsmechanismus der Dystrophin-mRNA reguliert, kann man auf diese Weise die Produktion von Utrophin in den Zellen kontrollieren. Dies stellt einen Anknüpfungspunkt für eine Therapie dar“, so Falcucci.
Didier Stainier, Direktor am Max-Planck-Institut, ordnet die Erkenntnisse der Studie ein: „Die transkriptionelle Adaptation ist ein faszinierender Prozess, der es uns erlaubt, die Folgen von Genmutationen zu entschärfen. Er glaubt deshalb, mit seinem Team das Verständnis über die Abläufe genetischer Kompensationen wie der transkriptionellen Adaptation in Zellen grundlegend verbessert zu haben. „Wir sind auch davon überzeugt, damit die Tür für die Entwicklung neuer therapeutischer Ansätze zur Behandlung der Duchenne Muskeldystrophie geöffnet zu haben. Insbesondere könnte dies für Patienten mit bislang schwer zu adressierenden Mutationen der Fall sein,“ so Stainier.